Признаки отравления фосгеном у человека
Содержание:
Обзор самых опасных отравляющих веществ
Химическое оружие, созданное на основе отравляющих веществ (ОВ), активно применялось в период Первой мировой войны. Массовое использование боевых отравляющих веществ (БОВ) официально прекращено с 1997 года, хотя негласно исследования в этой области продолжаются. Данные о новых разработках находятся под контролем спецслужб и редко становятся общедоступными. Среди ОВ, получивших огласку, наиболее опасными признаны препараты из следующего списка:
| VX, Ви-Экс, Ви-Икс, V-газ | Группа химических соединений с нервно-паралитическими (нейротоксическими) свойствами. Долгое время считалась наиболее токсичной из всех БОВ, изобретённых человеком. Внешне ви-газ напоминает густую, маслянистую, прозрачную жидкость с высокой степенью летучести. Вдыхание газа вызывает смерть уже спустя четверть часа, при контакте яда с кожей его действие замедляется вплоть до нескольких часов. При распространении на окружающей территории сохраняется на протяжении 1–2 недель. Наиболее известный случай применения связан с убийством брата Ким Чен Ына, правителя КНДР, в 2017 году. |
| Хлор | Одно из первых БОВ, применённых во время Первой мировой войны. Представляет собой пульмонотоксичный газ, при попадании в лёгкие вызывает сильный ожог тканей и удушье. При этом он является важным биогенным элементом, обнаружен в составе всех живых организмов на планете. Наиболее известный случай применения – битва при Ипре в 1915 году, начало массового использования химоружия (иприта) в ходе боевых действий. |
| Зарин | Прозрачная жидкость с нервно-паралитическими свойствами, легко растворяющаяся в воде. На территории способен сохраняться до 4-х часов после распространения. При среднесмертельной концентрации приводит к летальному исходу через минуту после вдыхания или контакта с кожей. Зарин был использован в ходе террористической атаки в токийском метро в 1994 году, а также во время боевой операции в Сирии (2013 год). |
| Зоман | Прозрачная жидкость с нервно-паралитическими свойствами, имеет запах яблок или свежескошенного сена. Более токсичный (в 2.5 раза) и более стойкий аналог зарина. Широко известных случаев применения официально не было. |
| Циклозарин | Нервно-паралитическое БОВ, в 4 раза токсичнее зарина. Представляет собой жидкость без цвета со сладковатым запахом, напоминающим аромат персиков. Разрешён к производству, хранению и использованию в исследовательских, но не в военных целях. |
| Фосген | Токсичный удушливый газ со специфическим запахом, напоминающим аромат прелого сена. Относится к категории удушающих БОВ, спустя четверть часа летальная концентрация приводит к отёку лёгких и смерти. Чрезвычайно опасен, но только при контакте с органами дыхания. Фосген широко использовался в ходе проведения боевых операций в начале прошлого века. |
| Адамсит | Жёлтый порошок, получил применение в виде аэрозолей во время Первой мировой войны. Оказывает влияние только на дыхательные пути, приводит к их сильному раздражению и удушью. Высокая концентрация этого вещества приводит к смерти спустя минуту после контакта. |
| Синильная кислота | Крайне летучая ядовитая жидкость с запахом горького миндаля. Вызывает гипоксию тканей внутренних органов, приводит к смерти спустя четверть часа. Применялась в 1916 году на реке Сомме, нацистами в концентрационных лагерях, а также в тюрьмах США при исполнении приговоров смертной казни вплоть до 1999 года. |
| Новичок | Относится к химическому оружию третьего поколения, состоит из относительно безвредных компонентов, или прекурсоров. При их соединении образуются боевые отравляющие вещества с высокой степенью токсичности. По некоторым данным, во время действовавшей в СССР программы Фолиант отравляющее вещество с бинарными свойствами было разработано группой исследователей, однако точные данные о нём относятся к государственной тайне. Новичок получил известность в 1995 году при отравлении российского банкира Ивана Кивелиди (яд был нанесен на телефонную трубку), а в 2018 году фигурировал в деле Скрипалей. |
| Полоний-210 | Чрезвычайно токсичное, канцерогенное и радиотоксичное вещество. В 4 трлн раз токсичнее, чем синильная кислота. Воздействует на печень, почки, селезёнку, костный мозг, а при тактильном контакте приводит к лучевому поражению кожи и всех внутренних органов. В качестве химического оружия не используется, однако получил известность при отравлении подполковника российской госбезопасности Александра Литвиненко в 2006 году. |
Симптомы и признаки поражения
Клиника отравления фосгеном состоит из следующих стадий или этапов, каждой из которых присущи свои характерные признаки.

Рефлекторная стадия возникает с первыми вдохами газа и проявляется:
- лёгким головокружением;
- режущим раздражением слизистых оболочек глаз и слезоточением;
- поверхностным, учащённым дыханием;
- першением в носоглотке или кашлем;
- стеснением в груди и/или тяжестью в эпигастральной области;
- иногда тошнотой и рвотой.
Скрытый этап мнимого благополучия является самым важным в оценке степени отравления этим газом. Несмотря на кажущееся отсутствие симптомов, они всё-таки есть:
- ритм дыхания учащён на фоне развивающейся брадикардии;
- уменьшается пульсовое давление;
- понижается верхнее и сохраняется нормальный уровень нижнего АД;
- при рентгене грудной клетки – выражено низкое стояние диафрагмы;
- при тихой перкуссии области сердца – уменьшение его абсолютной тупости;
- показатели гемоглобина и эритроцитов в общем анализе крови – понижены.
Во время мнимого благополучия врачу необходимо уточнить все детали нахождения в зоне поражения газом, в том числе, и суметь «различить» и оценить силу характерного запаха от волос или одежды.
Среднее время скрытого этапа – 4-6 часов, но возможные его колебания от 2 до 24 часов. Если в течение суток не наступило ухудшение и не развился отёк лёгких – прогноз является благоприятным. В противном случае наступает следующий этап развития отравления.
 На фото – применение химического оружия на поле боя
На фото – применение химического оружия на поле боя
Для стадии развития отёка лёгких или «утопления на суше» характерными являются следующие симптомы:
- сильное психоэмоциональное беспокойство;
- резкая головная боль;
- отдышка, удушье и асимметрия дыхания;
- острый бронхит или пневмония;
- кожные покровы синеют, особенно на лице и руках;
- по мере нарастания мелкопузырчатые хрипы в лёгких переходят в клокочущие;
- кашель с выхаркиванием пенистой мокроты (иногда с кровью) до 1,5 литров в сутки;
- t тела – 38-39°С;
- брадикардия сменяется тахикардией;
- верхнее АД держится на уровне 90 мм рт. ст.;
- мочеиспускание слабое, иногда полностью прекращено;
- потеря аппетита;
- запоры или поносы;
- в анализе крови – выраженный лейкоцитоз, высокие показатели гемоглобина и эритроцитов, эозинофилы – исчезают полностью, появляется ацетон.
С 3-го дня кривая летальных исходов резко падает, и наступает стадия регрессивного развития:
- постепенно исчезает синюшность и одышка;
- восстанавливается формула крови;
- снижается до нормальной температура тела;
- кашель, мокроты и хрипы – регрессируют.
Тем не менее, пребывание в стационаре больных со средней степенью поражения составляет от 10 до 20 дней.
Наиболее частыми последствиями и осложнениями, которые наблюдаются после поражения фосгеном, являются:
- бактериальная пневмония;
- выпотной плеврит;
- эмфизема легких,
- расширение сердца;
- тромбоз вен нижних конечностей.
Физические свойства
Фосген плохо растворяется в воде, не растворим в жирах и маслах; хорошо растворяется во многих органических растворителях (например, в бензине, ксилен, толуол) и сам может растворять значительное количество органических соединений. С неорганических соединений он растворяет только галогены и некоторые галогениды (AlCl 3, SbCl 3, SbCl 5). Фосген хорошо поглощается активированным углем — это свойство применяется при изготовлении противогазов.
Вещество является сильнолеткою: ее концентрация в воздухе при -40 ° C составляет 528 мг / м³, при -10 ° C — 2200 мг / м³, при -7,6 ° C — 4300 мг / м³.
Как можно заразиться
Как происходит отравление отравляющим газом? Выделяют несколько факторов интоксикации фосгеном. Факторы:
- аварийные ситуации на производстве,
- аварии транспорта, применяемого для перемещения газа,
- военные действия, при которых соединение используется в качестве отравляющего продукта.
Серьезные концентрации фосгена в воздухе провоцируют отравление у всех людей, находящихся в зоне поражения. При попадании внутрь вызывает отечность легочных тканей по медленному типу. Как действует фосген на органы? Газ не задерживается в дыхательных органах из-за неспособности растворяться в воде.
Понравится статья: «Отравление угарным газом – первая помощь и лечение«.
Поражение возникает при прямом действии на ткани легких, газ связывается с биологическими мембранами и провоцирует их гибель. Постепенно происходит гибель клеток легких, снижается объем специфического вещества, не дающего слипаться альвеолам. У человека возникает кислородное голодание.
При попадании на влажные кожные покровы не исключается возникновение раздражения и эритемы. При повышенной концентрации в воздухе возможно нарушение зрительной функции. Если есть прямой контакт с жидкой формой фосгена, отмечается обморожение и интенсивное раздражение
Использование промышленной формы соединения требует внимательности и осторожности. У детей отравление фосгеном развивается быстрее, чем у взрослых
Воздействие на организм и симптомы отравления
В виде газа фосген чрезвычайно токсичен для человека. Отравления жидкой формой, образующейся при температуре ниже 8.2 градуса, практически не встречаются. Основной путь интоксикации – ингаляционный.
Признаки отравления фосгеном проявляются не сразу, а по окончании скрытого периода – через 4–6 часов. В редких случаях возможно увеличение срока до 15 часов. Степень интоксикации зависит от продолжительности контакта с газом и его концентрации:
- При вдыхании низких концентраций (менее 0.004 мг/л) на протяжении 1-1.5 часов токсическое действие может и не проявиться.
- Содержание в воздухе 0.01 мг/л газа приводит к лёгкому отравлению. Если человек вдыхал пары менее часа, последствия интоксикации могут быть неощутимы или вовсе отсутствовать.
- Концентрация газа 0.022 мг/л при вдыхании более получаса летальна.
- Содержание фосгена свыше 0.1 мг/л при контакте от 30 до 60 минут приводит к гибели в 50% случаев. Оставшиеся 50% получают тяжёлые инвалидизирующие осложнения.
- Концентрация 1 мг/л смертельна при вдыхании более 5 минут. Если же содержание газа в окружающем воздухе составляет 5 мг/л, при его вдыхании смерть наступает в течение 2–3 секунд.
Во время латентного периода после контакта с отравляющим веществом развивается токсический отёк лёгких. Признаков ухудшения состояния не наблюдается, возможны лишь специфические проявления у людей с повышенной чувствительностью:
- неприятный вкус во рту;
- першение и жжение в носоглотке;
- воспаление слизистой оболочки глаз;
- тошнота;
- рвота;
- спазмы кашля;
- незначительные перебои дыхания и сердцебиения.
При прямом контакте с кожей развивается раздражение, переходящее затем в эритему — сильное покраснение из-за расширения капилляров. Также возникает обморожение различных частей тела.
 По окончании скрытой фазы интоксикации симптомы усиливаются. Кашель становится частым и интенсивным, синеет кожа на лице и губах, появляется одышка, снижается артериальное давление. Токсический отёк лёгких прогрессирует, что выражается такими симптомами:
По окончании скрытой фазы интоксикации симптомы усиливаются. Кашель становится частым и интенсивным, синеет кожа на лице и губах, появляется одышка, снижается артериальное давление. Токсический отёк лёгких прогрессирует, что выражается такими симптомами:
- мучительным давлением в области груди;
- сильным удушьем;
- учащённым дыханием – в 2–3 раза по сравнению с нормой;
- отхаркиванием вязкой, пенистой жидкости, смешанной с кровью.
Возможны и реакции со стороны других внутренних систем – нарушение стула (диарея или запор), затруднение мочевыделения, повышение температуры тела. При проведении лабораторных исследований в крови можно выявить кетоновые соединения.
Токсический отёк при отравлении фосгеном приводит к тому, что примерно половина крови, циркулирующей в организме, приливает в лёгкие. Из-за этого увеличивается их объем и масса. Затруднения дыхания вызывают у пострадавшего сильнейшее психоэмоциональное возбуждение: он начинает хватать ртом воздух, издаёт хрипы, и вскоре погибает.
Иногда при сильном отёке человек падает на землю и пытается не двигаться. У него сереет кожа и губы, появляется липкий холодный пот. Такое мучительное состояние длится несколько дней, затем заканчивается смертью.
При отравлении сверхвысокими концентрациями газа токсический отёк не развивается. Пострадавший падает на землю, бьётся в судорогах; его кожа быстро приобретает фиолетовый оттенок. Через несколько минут наступает смерть.
В редких случаях через 2–3 дня после отравления состояние пострадавшего может улучшиться: нормализуется температура, ритм дыхания, оттенок кожных покровов. Кашлевые позывы становятся менее выраженными и редкими, а хрипы в лёгких пропадают. Процесс восстановления дееспособности занимает не менее 3–4 недель.
Свойства[править | править код]
tкип= +8,2 °C, tпл= −118 °C, плотность в жидкой фазе 1,403 г/см³ (при температуре кипения), в газовой фазе 4,248 кг/м³ (+15 °C, 1 бар); плохо растворим в воде, хорошо — в органических растворителях.
Фосген представляет собой бесцветный газ, который ниже +8,2 °C конденсируется в бесцветную жидкость. Его запах напоминает прелые фрукты или сено. Технический продукт имеет слегка желтоватую или красновато-жёлтую окраску. Фосген примерно в 3,5 раза тяжелее воздуха. Из-за высокого давления пара он даже при низких температурах обладает большой летучестью. Фосген можно легко конденсировать сжатием, его критическая температура составляет 183 °C, критическое давление 56 кгс/см². В холодной воде фосген растворим мало −0,9 %. Он легко растворим в органических растворителях, например в бензине, толуоле, ксилоле, уксусной кислоте, хлороформе.
При обычной температуре фосген — стабильное соединение. При сильном нагревании он частично разлагается на хлор и окись углерода. Выше 800 °C он полностью диссоциирует. Количество ядовитых продуктов разложения при взрыве ничтожно, поэтому возможно применение фосгена во взрывных боеприпасах.
При хранении фосгена в стальных ёмкостях, например при длительном нахождении в минах, образуется пентакарбонил железа Fe(CO)5. Это — красновато-жёлтая жидкость, тяжелее фосгена, и разлагаемая на свету фотокаталитически с образованием ядовитой окиси углерода. Фосген почти не гидролизуется парами воды, поэтому концентрация фосгена в воздухе заметно падает лишь через длительное время. При высокой влажности воздуха облако фосгена за счёт частичного гидролиза может приобрести беловатый оттенок.
Энергично реагирует с аммиаком с образованием карбамида и хлорида аммония:
- COCl2+4NH3→(NH2)2CO+2NH4Cl.{\displaystyle {\mathsf {COCl_{2}+4NH_{3}\rightarrow (NH_{2})_{2}CO+2NH_{4}Cl}}.}
Эта реакция используется для экспресс-обнаружения утечек фосгена — смоченный водным раствором аммиака ватный тампон в присутствии фосгена начинает заметно выделять белый дым, состоящий из кристалликов хлорида аммония. Обнаружению фосгена этим способом мешает присутствие хлора, который с аммиаком также образует дым хлорида аммония.
Признаки отравления
Ещё раз повторим первые признаки отравления фосгеном:
- общая слабость;
- неприятный слабый привкус во рту;
- покраснение слизистых;
- першение в горле;
- головокружение;
- сухой кашель;
- замедление дыхания;
- тошнота, рвота — возможны при тяжёлом поражении.
Если первую помощь оказать своевременно и быстро, то человек не почувствует недомогания. Наступает первый период отравления – фаза мнимого благополучия. Её название полностью характеризует состояние человека в этот период – он чувствует себя хорошо, не замечает никаких отклонений. Если и проявляются какие-то реакции организма, будь то повышенная сонливость или слабость, их можно списать на стресс или нервное напряжение.

Первые признаки отравления фосгеном
Следом за бессимптомным периодом, примерно через 4-6 часов после отравления, наступает фаза клинических проявлений. Для неё характерны:
- нарастание пульса и артериального давления;
- урежение дыхания, одышка;
- сильный сухой кашель;
- боли за грудиной;
- головокружение;
- кожа и слизистые бледные с синюшным оттенком;
- появление патологических звуков при простукивании лёгких (может выявить специалист).
Яркая клиническая картина разворачивается, когда наступает отёк лёгких. При этом кашель становится влажным с обильным выделением мокроты до 1-1,5 литров за сутки. Один из основных признаков отёка лёгких – выделение изо рта вместе с кашлем кровавой пены.
Буквально на глазах у больного нарастает температура тела до 38-39°С. Дыхание становится шумным, с влажными хрипами. Больной непроизвольно принимает позу, в которой ему легче дышать – «позу собаки» — на четвереньках с опущенной вниз головой. Кожа и слизистые бледные до синюшности, ногтевые ложа багрово-синие.

Фосген — это опаснейший яд
С каждым часом такому больному становится хуже. Пульс нитевидный, плохо прощупывается, кровяное давление начинает снижаться, что нередко приводит к нарушению сознания.
Если в течение двух — трёх суток после появления признаков отёка лёгких больному не становится лучше, то исход чаще всего летальный.
Если же вторичные признаки отравления постепенно исчезают и состояние стабилизируется, отёк начинает спадать, то прогноз для жизни и здоровья благоприятный. Больной постепенно начинает выздоравливать. Улучшение состояния наблюдается в течение одной-двух недель.
Токсичность[править | править код]
Обладает удушающим действием. Смертельная концентрация 0,01—0,03 мг/л (при экспозиции 15 минут). Контакт фосгена с лёгочной тканью вызывает нарушение проницаемости альвеол и быстро прогрессирующий отёк лёгких. Антидот неизвестен.
Токсические свойстваправить | править код
Фосген очень ядовит, но только при вдыхании паров. Первые отчётливые признаки отравления появляются после скрытого периода от 4 до 8 часов; наблюдались даже периоды в 15 часов.
По различным данным вдыхание фосгена в концентрации 0,004 мг/л в течение 60—90 минут не приводит к отравлению.
Пребывание в атмосфере, содержащей до 0,01 мг/л фосгена, возможно максимально в течение 1 часа. При этом восприимчивые люди уже могут получить лёгкое отравление. Концентрации в 0,022 мг/л являются смертельными уже через 30 минут воздействия. В 50 % случаев отравление при вдыхании 0,1 мг/л в течение 30—60 минут приводит к смерти. Остальные 50 % оставшихся в живых длительно небоеспособны в результате тяжелейших отравлений. Даже при малом времени воздействия таких концентраций могут произойти сильные отравления, иногда заканчивающиеся смертью.
Концентрация 1 мг/л при времени экспозиции 5 минут в 50—75 % случаев отравления ведёт к смерти; меньшие концентрации (0,5—0,8 мг/л) приводят к тяжёлым отравлениям.
Концентрация 5 мг/л смертельна уже через 2—3 секунды[источник не указан 385 дней].
Малые концентрации фосгена влияют на вкусовые ощущения. Так, например, курить сигарету в содержащем фосген воздухе неприятно или вовсе невозможно.
Запах фосгена ощутим при концентрации 0,004 мг/л, однако на обонятельный нерв фосген влияет так, что в дальнейшем обоняние притупляется и перестают ощущаться даже более высокие концентрации. При опасной концентрации люди могут не почувствовать запах фосгена; его ПДК в воздухе рабочей зоны равна 0,5 мг/м3 (максимально-разовая).
Физиологическое действиеправить | править код
Токсический отёк лёгких, возникающий после вдыхания паров фосгена, дифосгена, трифосгена, проявляется лишь после скрытого периода в несколько часов. В этот период отравленный чувствует себя хорошо, и как правило вполне дееспособен. У восприимчивых людей в это время появляется сладкий привкус во рту, иногда тошнота и рвота. В большинстве случаев возникают незначительные позывы к кашлю, першение и жжение в носоглотке, небольшие нарушения ритма дыхания и пульса.
После латентного периода наступает сильный кашель, одышка, синюшность лица и губ.
Прогрессирующий отёк лёгких ведёт к сильному удушью, давлению в грудной клетке, ритм дыхания увеличивается от 18—20 в минуту (норма) до 30—50 в минуту, в кризисе — до 60—70 в минуту. Дыхание судорожное. Содержащая белок отёчная пенистая и вязкая жидкость выбрызгивается из альвеол и бронхиол в более широкие дыхательные пути, ведёт к затруднению и невозможности дыхания. Отравленный отхаркивает большие количества этой жидкости, часто смешанной с кровью. При токсическом отёке лёгких примерно до половины общего количества крови организма переходит в лёгкие, которые в результате этого опухают и увеличиваются в массе. В то время как нормальное лёгкое весит около 500—600 грамм, можно наблюдать «фосгеновые» лёгкие весом до 2,5 килограмм.
Затем кровяное давление резко падает, отравленный пребывает в сильнейшем возбуждении, дышит с шумом, хватает ртом воздух, затем наступает смерть.
Встречаются случаи, когда отравленный избегает любого лишнего движения и для облегчения дыхания выбирает какое-то наиболее удобное положение. Губы у таких отравленных серые, пот холодный и липкий. Несмотря на удушье, мокрота у них не отделяется. Через несколько дней отравленный умирает.
Редко, через 2—3 суток может наступить улучшение состояния, которое через 2—3 недели может закончиться выздоровлением, но часты осложнения в результате вторичных инфекционных заболеваний, что приводит к смертельному исходу.
При очень высоких концентрациях отёк лёгких не развивается. Отравленный делает глубокие вдохи, падает на землю, корчится и бьётся в судорогах, кожа на лице становится от фиолетово-синей до тёмно-синей, и очень быстро наступает смерть.
Хеглер на примере одного поражения так описывает характер отравления фосгеном:
Один из известных токсикологов Мунтш так описывал состояние поражённого фосгеном человека:
Нуклеофильное замещение хлора
Фосгенирование спиртов и карбоновых кислот
Фосгенирование спиртов и фенолов ведёт к образованию хлорформиатов, которые, в свою очередь, могут быть выделены, либо превращены в соответствующие карбонаты при проведении реакции с избытком спирта:
-
- COCl2→−HClROHROCOCl→−HClROHROCOOR{\displaystyle {\mathsf {COCl_{2}{\xrightarrow{ROH}}ROCOCl{\xrightarrow{ROH}}ROCOOR}}}
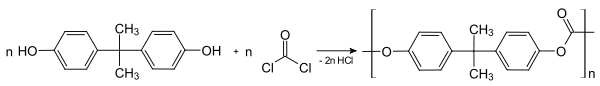
Реакция проводится при повышенной температуре в присутствии третичных аминов, которые связывают выделяющийся HCl; фосгенирование диолов приводит к образованию олигомеров и полимеров, в частности, фосгенирование бисфенола А является промышленным методом синтеза поликарбонатов:
Фосгенирование карбоновых кислот с хорошим выходом ведёт к хлорангидридам:
-
- RCOOH+COCl2→RCOCl+HCl+CO2{\displaystyle {\mathsf {RCOOH+COCl_{2}\rightarrow RCOCl+HCl+CO_{2}}}}
Фосгенирование аминов
Фосгенирование вторичных аминов ведёт к карбамоилхлоридам, которые в случае вторичных аминов являются стабильными:
-
- R2NH+COCl2→R2N-COCl+HCl{\displaystyle {\mathsf {R_{2}NH+COCl_{2}\rightarrow R_{2}N{\text{-}}COCl+HCl}}}
В случае первичных и третичных аминов карбамоилхлориды, получающиеся при их фосгенировании, нестабильны, и, хотя в определённых условиях могут быть выделены, претерпевают дальнейшие превращения.
В случае первичных аминов карбамоилхлориды элиминируют HCl с образованием изоцианатов, при этом ароматические амины менее реакционноспособны и их карбамоилхлориды более стабильны:
-
- RNH2+COCl2→RNHCOCl+HCl{\displaystyle {\mathsf {RNH_{2}+COCl_{2}\rightarrow RNHCOCl+HCl}}}
-
- RNHCOCl→RNCO+HCl{\displaystyle {\mathsf {RNHCOCl\rightarrow RNCO+HCl}}}
Этот метод является основным промышленным методом синтеза изоцианатов.
В случае третичных аминов при фосгенировании образуются нестабильные четвертичные соли, распадающиеся с образованием карбамоилхлорида и алкилгалогенида:
-
- R3N+COCl2→R3NCOCl+Cl−→R2NCOCl+RCl{\displaystyle {\mathsf {R_{3}N+COCl_{2}\rightarrow ^{+}Cl^{-}\rightarrow R_{2}NCOCl+RCl}}}
При избытке первичного или вторичного амина образуются замещённые производные мочевины вследствие реакции изоцианатов либо карбамоилхлоридов с присутствующим в реакционной смеси амином:
-
- RNCO+RNH2→RNHCONHR{\displaystyle {\mathsf {RNCO+RNH_{2}\rightarrow RNHCONHR}}}
- R1R2NCOCl+R1R2N→R1R2NCONR1R2+D{\displaystyle {\mathsf {R^{1}R^{2}NCOCl+R^{1}R^{2}N\rightarrow R^{1}R^{2}NCONR^{1}R^{2}+D}}}
Фосгенирование амидов
Фосген реагирует с незамещенными амидами карбоновых кислот, действуя как дегидратирующий агент, при этом образуются нитрилы:
-
- RCONH2+COCl2→RCN+2HCl+CO2{\displaystyle {\mathsf {RCONH_{2}+COCl_{2}\rightarrow RCN+2HCl+CO_{2}}}}
Взаимодействие фосгена с N-монозамещенными формамидами ведет к изонитрилам:
-
- RNHCHO+COCl2→RNC+2HCl+CO2{\displaystyle {\mathsf {RNHCHO+COCl_{2}\rightarrow RNC+2HCl+CO_{2}}}}
Взаимодействие фосгена с N-монозамещенными амидами ведет к имидоилхлоридам:
-
- RCONHR+COCl2→RCCl=NR+HCl+CO2{\displaystyle {\mathsf {RCONHR+COCl_{2}\rightarrow RCCl{\text{=}}NR+HCl+CO_{2}}}}
При фосгенировании N-дизамещенных амидов образуются ионные хлориды четвертичных имидоилхлоридов, эта реакция лежит в основе модифицированного метода формилировании по Вильсмейеру — Хааку. В этом варианте метода вместо комплекса диметилформамида с оксихлоридом фосфора в качестве формилирующего агента используется продукт фосгенирования диметилформамида и дальнейшего декарбоксилирования диметилформамида — четвертичный имидоилхлорид:
-
- (CH3)2NCHO+COCl2→(CH3)2N+=CH-O-COClCl−{\displaystyle {\mathsf {(CH_{3})_{2}NCHO+COCl_{2}\rightarrow Cl^{-}}}}
-
- (CH3)2N+=CH-O-COClCl−→(CH3)2N+=CHClCl−+CO2{\displaystyle {\mathsf {Cl^{-}\rightarrow Cl^{-}+CO_{2}}}}
Этот имидоилхлорид менее активен, чем классический реагент Вильсмейера, однако достаточно реакционноспособен для формилирования активированных ароматических соединений:
-
- ArH+(CH3)2N+=CHClCl−→Ar-CH=N+(CH3)2Cl−+HCl{\displaystyle {\mathsf {ArH+Cl^{-}\rightarrow Cl^{-}+HCl}}}
-
- Ar-CH=N+(CH3)2Cl−+H2O→ArCHO+(CH3)2NH2Cl{\displaystyle {\mathsf {Cl^{-}+H_{2}O\rightarrow ArCHO+Cl}}}