Что делать при отравлении щелочью в первую очередь?
Содержание:
Как утилизировать щелочь на производстве
Утилизация щелочей производится в три этапа:
Транспортировка. Отработанные щелочи перевозятся в специально предназначенные для последующей утилизации места. При этом перевозка производится транспортом, который оснащен специализированным оборудованием. На такой транспорт помещают герметично закрытые баки с щелочными отходами. Герметичность необходима для того, чтобы не происходил контакт перевозимых отходов с другими соединениями. Эти баки устанавливаются в вертикальном положении и нумеруются.
Утилизация. Осуществляют реакцию нейтрализации, для этого используют кислоты. При реакции может происходить выделение достаточно большого количества теплоты в зависимости от выбранных реагентов
В связи с этим важно, чтобы процесс осуществлял специально обученный человек, соблюдая технику безопасности.
Переработка продуктов реакции. Образующиеся в результате реакции нейтрализации соли отправляются на дальнейшую переработку с целью последующего использования их в быту и производстве.

Тому, как осуществляется утилизация кислоты (в домашних условиях), использующейся в качестве электролита, посвящено следующее короткое видео:
Правильная утилизация кислот и щелочей – крайне важный процесс, позволяющий защищать природную среду и здоровье человека от негативного влияния агрессивных сред. Утилизировать такие опасные вещества можно самостоятельно, однако лучше все-таки пользоваться услугами профессионалов.
Химическая формула пищевой соды
Несмотря на то, что пищевая сода имеет такое простое название, с точки зрения химии, она представляет собой сложное соединение, обозначаемое химической формулой NaHCO3. Из этой записи становится понятно, что кислая соль угольной кислоты, которой по сути и является пищевая сода, в структурном плане состоит из молекулы натрия, водорода и углерода (по одной), а также из 3-х молекул кислорода. Если суммировать атомные веса данных компонентов, в результате получается атомная масса порошка, которая равна 84 а. е.
В сфере кулинарии нередко можно услышать и другие термины – питьевая, чайная сода. Всё это названия, которые служат для обозначения одного того же порошка – гидрокарбоната натрия.
Формула реакции пищевой соды и уксуса
Каждой хозяйке знакома уловка с соединением пищевой соды и уксуса для хорошего поднятия выпечки. Конечно, многие рецепты дают указание и на добавление одной лишь соды, однако в таком случае тесто получается темнее обычного, а его привкус приобретает странноватое подобие мыла. Что же происходит при взаимодействии этих двух компонентов? Кислота, воздействуя на щёлочь, приводит к выделению в процессе реакции углекислого газа. Когда тесто находится в духовом шкафу, образование углекислоты усиливается, поэтому выпечка по итогу становится рыхлой и пышной. Из этого следует, что соду необходимо гасить не в ложке, как это делают многие хозяйки, а непосредственно в самой муке. Для этого тесто рекомендуется замешивать в двух тарелках: в одну из них нужно добавлять только сухие ингредиенты, в том числе и содовый порошок, а в другую – вместе с уксусом вливать жидкости, после чего соединять содержимое обеих ёмкостей. Подобный подход позволит предотвратить осуществление необходимой реакции до момента введения соды и уксуса в тесто, в результате чего разрыхление теста произойдёт в разы эффективнее обычного.
Видео — Что будет если смешать 3 кг соды с уксусом
Формула реакции пищевой соды и лимонной кислоты
Кроме питьевой соды и уксуса, в кулинарии и быту используется ещё одно вещество – лимонная кислота. Все эти 3 компонента являются главными составляющими рецептов, информирующих не только о способах поднятия выпечки, но и методах качественной чистки стойких загрязнений на посуде, в поверхностях холодильника и шкафчиков.
А вот для очищения водопроводных кранов и тарелок из нержавейки используется именно дуэт соды и лимонной кислоты: компоненты соединяют между собой, после чего в полученном веществе смачивают салфетку и протирают ей те места, которые требуют удаления грязи.
Сочетание гидрокарбоната натрия и лимонного сока становится актуальным при выведении пятен с одежды. Оба ингредиента, взятых в равных пропорциях, добавляют в замоченное бельё и оставляют буквально на полчаса, по истечению которого приступают к стирке.
Во время взаимодействия чайной соды и лимонной кислоты возникает соль цитрат натрия, углекислый газ и вода. При смешивании данных ингредиентов в кипящей воде реакция имеет свойство происходить достаточно бурно.
Мнение специалистов
Клинические исследования, проводимые при участии союза Педиатров России, позволили установить, что:
- При применении комплекса средств ТМ «Ла-Кри» уровень влажности кожи снизился на 4% в сравнении, а у группы применявшей Плацебо уровень влажности снизился на 9%.
- При применении комплекса средств ТМ «Ла-Кри» уровень кислотности кожи повысился на 1% в сравнении, а у группы применявших Плацебо уровень кислотности снизился на 1%, при этом у второй группы испытуемых начальное значение кислотности кожи было значительно выше.
- Показатели влажности кожи незначительно снизились и остались в зоне дегидратации, однако при использовании ТМ «Ла-Кри» показатели оставались значительно лучше, чем у группы, применявшей Плацебо. Уровень кожного жира в целом изначально был низким, и по итогу в группе, применявшей альтернативные средства для ухода за кожей, он снизился практически в 2 раза, а в группе, использовавшей ТМ «Ла-Кри» он остался на неизменном уровне.
- При оценке динамики показателей эпидермального барьера с помощью диагностической шкалы EASI у группы пациентов применявших продукцию ТМ «Ла-Кри» средний процент улучшения при прохождении полного курса составил 28% и только 9% пациентов без изменения, при этом у группы применявшей «Плацебо» у 13% пациентов отметилось улучшение и у 56% пациентов без изменения.
Первая медицинская помощь
Неотложная помощь при кислотных ожогах помогает повысить эффективность последующего лечения и избежать развития опасных для жизни осложнений. Человек, оказывающий помощь пациенту, должен иметь знания о химических ожогах и способах борьбы с проблемой согласно алгоритму оказания неотложной помощи:
- Прекращение влияния химиката на кожу или слизистые. Если кислота попала на одежду или нижнее белье, ткань разрезают и снимают. Если на коже присутствуют остатки кристаллического химиката, их стряхивают, потом смывают. Пораженную область тщательно промывают под струей воды, чтобы снизить концентрацию кислоты. Рану следует промывать не менее 30 минут.
- Нейтрализация кислоты. Считается, что при кислотном ожоге кожу необходимо промыть щелочным раствором, но так делать не стоит. Только специалисты с профильным образованием могут определить, каким раствором правильно воздействовать на ожог. Сегодня химсредства — сочетания разных компонентов, а не одной конкретной кислоты, и подбирать состав для нейтрализации самостоятельно опасно. В качестве первой помощи достаточно подержать поврежденный участок кожи под проточной водой долгое время.
- Наложение стерильной повязки. После удаления агрессивного вещества на кожу накладывают сухой стерильный бинт. Применять вату для обработки пораженных областей нельзя.
- Введение обезболивающих средств. При наличии выраженного болевого синдрома делают укол Анальгина.
- Обеспечение специального питьевого режима. До приезда бригады «Скорой помощи» человеку каждые 15 минут дают чай или негазированную минеральную воду.
Сильные кислоты и сильные основания
Сильная кислота является тот , который полностью диссоциирует в водном растворе. Например, соляная кислота HCl — сильная кислота.
- HCl (водн.) → H + (водн.) + Cl — (водн.)
Сильное основание является тот , который полностью диссоциирует в водном растворе. Например, гидроксид натрия , NaOH, является сильным основанием.
- NaOH (водн.) → Na + (водн.) + OH — (водн.)
Следовательно, когда сильная кислота реагирует с сильным основанием, реакцию нейтрализации можно записать как
- Н + + ОН — → Н 2 О
Например, в реакции между соляной кислотой и гидроксидом натрия ионы натрия и хлора, Na + и Cl — не принимают участия в реакции. Реакция согласуется с определением Бренстеда-Лоури, потому что в действительности ион водорода существует как ион гидроксония , так что реакцию нейтрализации можно записать как
- Н 3 О + + ОН — → Н 2 О + Н 2 О → 2 Н 2 О
Когда сильная кислота нейтрализуется сильным основанием, в растворе не остается лишних ионов водорода. Раствор считается нейтральным, так как он не является ни кислотным, ни щелочным. РН такого раствора близка к значению 7; точное значение pH зависит от температуры раствора.
Нейтрализация — экзотермическая реакция. Стандартное изменение энтальпии для реакции H + + OH — → H 2 O составляет -57,30 кДж / моль.
Количественное лечение
Термин « полностью диссоциированный» применяется к растворенному веществу, когда концентрация продуктов его диссоциации ниже пределов обнаружения , то есть когда концентрации продукта слишком низки для измерения. Количественно это выражается как log K <-2, или в некоторых текстах log K <-1,76. Это означает, что значение константы диссоциации не может быть получено из экспериментальных измерений. Однако это значение можно оценить теоретически. Например, значение log K ≈ -6 было оценено для хлористого водорода в водном растворе при комнатной температуре. Следовательно, химическое соединение может вести себя как сильная кислота в растворе, когда его концентрация низкая, и как слабая кислота, когда ее концентрация очень высока. Серная кислота является примером такого соединения.
Слабые кислоты и сильные основания
Слабая кислота является тот , который не диссоциирует полностью , когда он растворен в воде. Вместо этого образуется равновесная смесь.
- АН + Н 2 О ⇌ Н 3 О + + А —
Уксусная кислота является примером слабой кислоты. PH нейтрализованного раствора не близок к 7, как в случае сильной кислоты, но зависит от константы кислотной диссоциации , K A , кислоты. Значение pH в конечной точке или точке эквивалентности титрования можно легко рассчитать. В конечной точке кислота полностью нейтрализуется, поэтому аналитическая концентрация ионов водорода, T H , равна нулю, а концентрация конъюгированного основания, A — , равна аналитической концентрации кислоты; написание АГ для кислоты, = Т . Когда раствор кислоты AH находится в равновесии , по определению концентрации связаны выражением
- = K a ; p K a = — log 10 K a
Растворитель (egwater) опущен из определяющего выражения в предположении , что его концентрация очень много больше , чем концентрация растворенной кислоты, [H 2 O] >> T A .
- K w = ; p K w = −log 10 K w
уравнение баланса масс в ионах водорода легко записать.
- T H = + K a —K w
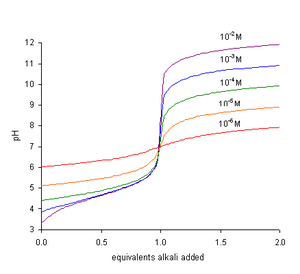
Кривые титрования для добавления сильного основания к слабой кислоте с p K a 4,85. На кривых указана концентрация кислоты.
K w представляет собой константу самодиссоциации воды, K W = . СеместрK wравна концентрации гидроксид-ионов. При нейтрализации T H равна нулю. После умножения обеих частей уравнения на получается
- 2 + K a T A 2 — K w = 0
и после перестановки и логарифмирования
- pH = 12p K w -12 журнал (1 + Т АК а)
В разбавленных растворах кислоты срок 1 + Т АК а равно Т АК а с хорошим приближением.
Это уравнение объясняет следующие факты:
- PH в конечной точке зависит главным образом от силы кислоты, p K a .
- РН в конечной точке зависит также от концентрации кислоты, T A .
При титровании слабой кислоты сильным основанием pH возрастает более круто по мере приближения к конечной точке. Наклон кривой pH в зависимости от количества титранта является максимальным, когда pH численно равен значению pK a . Конечная точка наступает при pH выше 7. Поэтому наиболее подходящим индикатором для использования является такой индикатор , как фенолфталеин , который меняет цвет при высоком pH.
Ожог кислотой: первая помощь
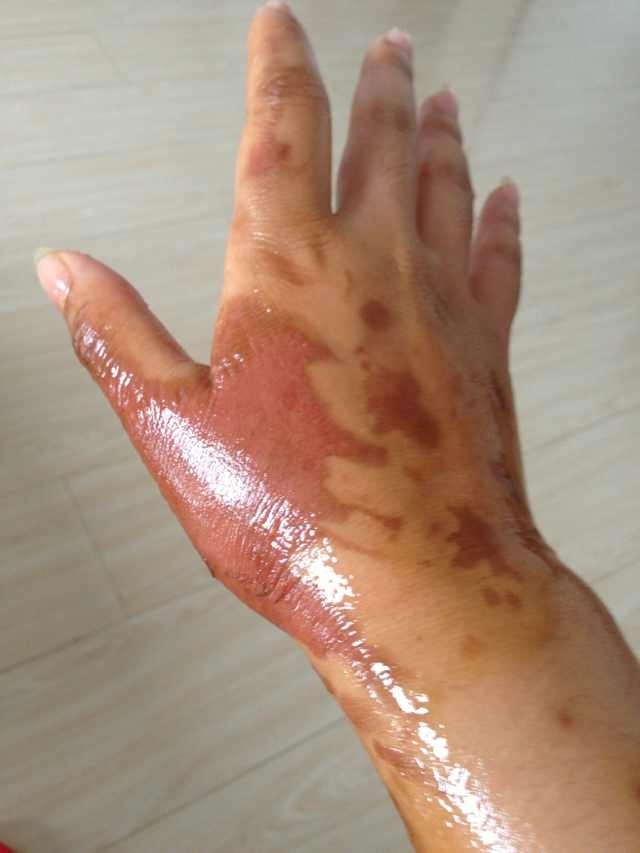
Данный химикат применяется в нефтяной, кожевенной, металлообрабатывающей, пищевой (в качестве эмульгатора) химической и аграрной промышленности (в составе минеральных удобрений). При контакте с кожными покровами вызывает окрашивание кожи в белый цвет, после чего образуется коричневый оттенок.
При контакте с кожей, слизистыми, а также при вдыхании паров данного вещества можно получить ожог кислотой. Лечение сводится к описанным выше рекомендациям.
Ожог борной кислотой
Данное вещество используется в основном в медицине, фотографии, пищевой промышленности и некоторых других отраслях. Если вы обожглись им, срочно проведите описанные выше процедуры по оказанию первой помощи.
Ожог лимонной кислотой
Этот химикат применяется в кулинарии, пищевой промышленности, при производстве косметики. При употреблении внутрь в больших дозах способен привести к повреждениям пищевода.
Ожоги азотной кислотой
При контакте с этим веществом кожа приобретает желтый цвет. Возможно появление долгозаживающих язв, поэтому необходимо как можно скорее оказать пострадавшему первую помощь.
Химический ожог соляной кислотой: первая помощь
Это едкое вещество используют в пищевой и гидрометаллургической промышленности, а также в медицине. При попадании на кожный покровы вызывает сильное жжение и образование струпов. Поддается нейтрализации раствором соды.
Чем лечить ожог от уксусной кислоты?
Водные растворы этого вещества используются в кулинарии, бытовой консервации, в ремонтных работах (например, при крашении), книгопечатании, в качестве растворителя, при получении некоторых фармацевтических препаратов. Обожженный участок тела нужно обработать так же, как и в описанных выше случаях.
Ожог уксусной кислотой и его особенности
Что делать при ожоге уксусной кислотой? Лечение должно проходить по описанному выше принципу
Обратите внимание на то, что последствия ожога кожи уксусной кислотой могут быть очень опасными (вплоть до некроза тканей), так что первую помощь необходимо оказать незамедлительно!. Если пострадавший принял химикат внутрь, может пострадать гортань (ее повреждение способно привести к нехватке воздуха), слизистая оболочка рта, пищевод, желудок
Не рекомендуется вызывать рвоту, так как повторное прохождение химиката через ЖКТ приводит к очень тяжелым последствиям. Требуется дать пострадавшему большое количество питья и как можно быстрее доставить в больницу, где ему введут зонд и промоют желудок.
Если пострадавший принял химикат внутрь, может пострадать гортань (ее повреждение способно привести к нехватке воздуха), слизистая оболочка рта, пищевод, желудок. Не рекомендуется вызывать рвоту, так как повторное прохождение химиката через ЖКТ приводит к очень тяжелым последствиям. Требуется дать пострадавшему большое количество питья и как можно быстрее доставить в больницу, где ему введут зонд и промоют желудок.
Хирургическое вмешательство
Оперативное лечение используется, только если другие методы не дают нужный результат. Для каждого конкретного пациента выбирается способ операции в зависимости от тяжести поражения. Существует несколько видов:
- Некротомия. Удаляются измененные ткани. Операция предотвращает распространение некроза и дает возможность восстановления тканям и кровоснабжению на поврежденном участке.
- Некрэктомия проводится преимущественно при 3 степени и небольшой площади поражения. Рана основательно чистится для предотвращения гнойных процессов и быстрого восстановления.
- Частичная некрэктомия. Оперативное вмешательство аналогичное некректомии. Проводится в щадящем режиме, частями. Помогает легче переносить очищение ран больших по площади поражений.
- Трансплантация кожи. При обширных травмах осуществляется пересадка кожи.
- Ампутация. Проводится при очень тяжелых поражениях для предотвращения прогресса отмирания тканей.
Кислоты и щелочи в природе
Ты уже успел убедиться в том, что вокруг нас — огромное количество кислот и щелочей. Молочные продукты, овощи и фрукты содержат лимонную, яблочную, щавелевую, уксусную, молочную, аскорбиновую и другие кислоты. Трудно поверить, но в косточках вишен и миндаля содержится (хоть и в минимальных количествах) такой сильный яд, как синильная кислота! Известно, что многие насекомые предпочитают защищаться разными кислотами. Никогда не задумывался, почему укусы обыкновенного крошечного муравья бывают такими болезненными? А все потому, что он вспрыскивает в ранку капельки муравьиной кислоты. Эту же кислоту выделяют и кое-какие виды гусениц, а тропические пауки и некоторые жуки защищаются от врагов при помощи уксусной и серной кислот.
Что будет, если выпить щелочь?
У выпившего щелочь человека наблюдается следующая симптоматика:
- Ожог рта. Мягкие ткани отекают и приобретают красный цвет. Человек страдает от сильной боли. Постепенно отеки преобразуются в язвы;
- Появляется жажда. Во рту долго стоит металлический привкус;
- Боль в области груди. Ее интенсивность зависит от концентрации выпитой щелочи;
- Сильная рвота с вкраплениями крови. Связано это с тем, что щелочь повреждает внутренние сосуды;
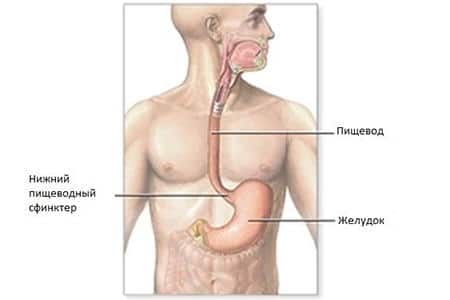
- Риск асфиксии из-за интенсивной рвоты или деформированных пищеводных тканей;
- Состояние шока. Если концентрация щелочи высока, то болевой симптом приводит к исступлению человека, он перестает разумно мыслить и порой даже не в состоянии вызвать медиков;
- Спустя какое-то время после первичных симптомов наступает кровавый понос.
Анализируя случаи отравления щелочью, врачи пришли к выводу, что желудок может вовсе не пострадать. Ведь при взаимодействии выпитой щелочи с кислотной средой желудка происходит нейтрализация первой.
Но если концентрация вещества достаточно высока, то есть вероятность перфорации пищевода, то есть образования в нем отверстия.
Даже употребление небольших доз щелочных растворов чревато осложнениями, хотя поначалу человек может отделаться слабовыраженными симптомами. Поэтому никакого самолечения, только оперативное обращение к врачу.
Также специалисту нужно сообщить название вещества, ставшее причиной отправления. Это поможет сразу подобрать курс лечения и не тратить время на дополнительные обследования.
Часто впавшие в шоковое состояние пострадавшие совершают ряд опасных ошибок:
- Вызывают рвоту. Она в несколько раз повышает риск повреждения пищевода. Ведь щелочная жидкость из желудка вновь пойдет назад по тому же пути, что попала внутрь;
- Употребляют слабительные. Только врач может решить, насколько целесообразен тот или иной метод детоксикации;
- Пьют раствор лимонной кислоты. Эта ошибка связана с тем, что люди имеют общие представления о нейтрализации щелочи кислотой. Но то, что актуально для бытового применения, никак не поможет при отравлениях. Кислотный раствор может дать лишь дополнительную нагрузку на отравленный организм.
Лечение ожога щелочью
Доврачебная помощь при ожогах щелочью
Первая помощь при ожогах щелочью заключается:
- в незамедлительном промывании пораженных участков кожи холодной проточной водой, которое проводится не менее 15 минут;
- в обработке обмытых водой обожженных мест одним из подкисляющих растворов: 2% раствором лимонной или борной кислоты (на 250 мл воды ½ чайной ложки); 1% раствором уксусной кислоты; раствором из смеси 9%-го столового уксуса с водой (в соотношении 1:3).
Доврачебная помощь при ожогах щелочью в порошкообразном виде следует начинать с его тщательно удаления с кожи в сухом виде, и только после этого можно промывать поврежденный участок водой и подкисленным раствором. Учтите, что растворение сухой щелочи в воде запускает ее повреждающее воздействие на кожу.
Если ожог вызван негашеной известью, промывать его водой нельзя ни в коем случае. Нужно убрать щелочь, обработав кожу с помощью любого растительного масла с последующим накладыванием сухой стерильной салфетки.
При воздействии на кожу гашеной извести следует после промывания водой несколько раз обмыть пораженное место подслащенной водой (столовая ложка сахара без горки на 250 мл воды). Можно делать этим раствором примочки.
Ожог глаз щелочью также нужно несколько минут промывать холодной водой (только под струей), после чего следует продолжать промывание глаз 2% раствором борной или лимонной кислоты. В данном случае необходимо в срочном порядке обращаться в лечебное учреждение.
, , ,
Лечение ожога щелочью в стационаре
В легких случаях повреждения верхнего слоя кожи лечение ожога щелочью можно проводить, используя всем известный аэрозоль Пантенол, линимент синтомицина, а также спрей Оксициклозоль (с антибиотиком окситетрациклином и кортикостероидом преднизолоном), антисептические лекарства в виде растворов для местного использования Диоксизоль или Новоиманин.
Диоксизоль содержит антибактериальное средство диоксидин и обезболивающий лидокаин. Препарат применяют не только для борьбы с инфекцией, но и для стимулирования процессов репарации в ожоговой ране, для чего им обрабатывается поврежденный участок и смачивается повязка – один раз в течение дня. Процедура может сопровождаться небольшим жжением, а вот длительное использование данного раствора может вызвать побочный эффект в виде крапивницы. При проблемах с сердцем (брадикардии), низком АД и беременности Диоксизоль противопоказан.
1% спиртовой экстракт зверобоя – Новоиманин – помогает при нагноении ожоговой раны (подсушивая ее) и хорошо снимает воспаление. Для промывания раны или смачивания повязки его нужно разводить водой (на 5 частей 1 часть экстракта).
И в домашних условиях, и в больницах используется такая эффективная лекарственная форма, как мазь (или гель). Врачи рекомендуют при ожогах любой этиологии антибактериальные мази Левомеколь и Левосин (с левомицетином), Стрептонитол (с сульфаниламидами), Сульфаргин (с сульфатиазолом серебра) и др. Полная информация в материале – Мазь от ожогов.
А о том, какие методы используются в лечении ожогов средней и тяжелой степени, можно узнать из отдельной публикации – Лечение ожогов
Народное лечение
Применяя народное лечение в виде компрессов и примочек, следует помнить о соблюдении правил антисептики. Поэтому лучше всего использовать отвары лекарственных растений, а не средства, которые готовятся без термической обработки (то есть могут стать источником инфицирования ожоговой раны).
Рекомендуемое народное лечение травами включает отвары цветков календулы, травы зверобоя, листьев подорожника, лапчатки, донника. Хорошо снимает воспаление крепкий отвар лаврового листа (5-6 листьев на стакан кипятка). Травяные отвар готовятся из расчета столовая ложка сырья на 200-250 мл кипятка (кипятят примерно 10-12 минут); после настаивания отвара им промывают ожоговые раны при смене повязки (1-2 раза в день).
Хорошо вытягивает гной сок алоэ; подсушивает мокнущую рану сок чистотела (разбавленный кипяченой водой 1:1); помогает снять воспаление эфирное масло кедра, эвкалипта, чайного дерева; ускоряет заживление ожога щелочью примочки с соком из листьев и стеблей золотого уса (каллизии душистой), прополис, мумие.
, , , , , ,
Симптомы
Общая клиническая картина и симптомы при химическом ожоге может существенно отличаться в зависимости от глубины поражения кожи и типа реагента. Всего в медицинской практике выделяют четыре основных степени травмы.
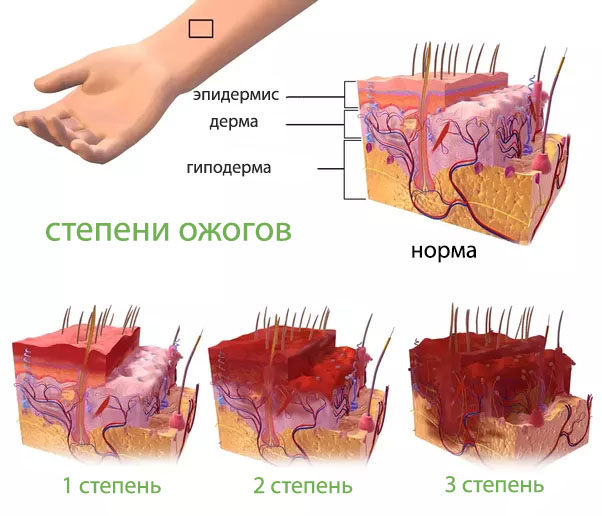
Первая степень
Это легкая форма заболевания, не требующего медицинского вмешательства (например, ожоги серной кислотой). Ожог первой степени может спровоцировать попадание химического вещества в небольшом количестве. При химическом ожоге кожи первой степени характерны такие симптомы:
- покраснение кожи в месте контакта с химическим веществом;
- гипертермия поврежденного участка;
- незначительный отек;
- боль средней интенсивности длительностью до нескольких часов;
- зуд и легкое жжение;
- шелушение кожи на второй-третий день после получения травмы.
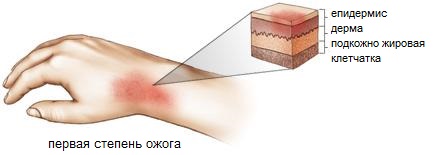 Обычно признаки химического ожога сохраняются в течение 2-5 дней. Чтобы ускорить процесс заживления раны и предотвратить развитие осложнений, достаточно элементарных мер по оказанию первой помощи.
Обычно признаки химического ожога сохраняются в течение 2-5 дней. Чтобы ускорить процесс заживления раны и предотвратить развитие осложнений, достаточно элементарных мер по оказанию первой помощи.
Вторая степень
Симптомы при ожоге щелочью или кислотой второй степени не несут большой угрозы здоровью пациента. Для этой формы характерны такие же проявления заболевания, как и при химическом ожоге первой степени. Основное отличие – формирование волдырей, заполненных прозрачной или слегка мутной жидкостью. Размеры пузырей могут варьироваться в пределах нескольких сантиметров в зависимости от количества химического вещества, попавшего на кожу, и свойств самого эпидермиса.
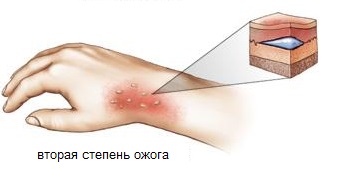 Лечение химического ожога проводится амбулаторно. Первую повязку накладывает медицинский сотрудник, дальнейшую смену повязок пациент может проводить самостоятельно. Прокалывать волдыри самостоятельно запрещено, так как это может привести к инфицированию раны. При подозрении на гнойное воспаление, пузыри вскрываются в стерильных условиях. В таких случаях дальнейшее лечение включает антибактериальную терапию.
Лечение химического ожога проводится амбулаторно. Первую повязку накладывает медицинский сотрудник, дальнейшую смену повязок пациент может проводить самостоятельно. Прокалывать волдыри самостоятельно запрещено, так как это может привести к инфицированию раны. При подозрении на гнойное воспаление, пузыри вскрываются в стерильных условиях. В таких случаях дальнейшее лечение включает антибактериальную терапию.
Третья/четвертая степень
Это тяжелая форма заболевания, несущая угрозу жизни пациенту при несвоевременном оказании первой помощи. Из-за омертвления тканей самостоятельное восстановление кожи чаще всего невозможно. Тщательное медицинское обследование с дальнейшим лечением в стационаре – обязательные условия полного выздоровления пациента.
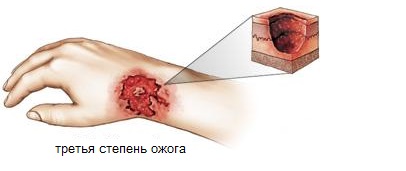
Симптомы химических ожогов кислотой и щелочных ожогов будут зависеть, в первую очередь, от типа вещества, попавшего на кожу. Для кислотных ожогов характерны раны средней глубины, покрытые плотной коркой. Ожог серной кислотой образует рану белесого оттенка с постепенным переходом в серый. При воздействии азотной кислоты рана приобретает желто-зеленый оттенок. Формирование желтого струпа свойственно контакту кожи с соляной кислотой. В тоже время попадание на кожу щелочных составов характеризуется формированием влажной раны с белесоватым налетом на дне.
В зависимости от количества реагента и длительности его воздействия на ткани могут отмечаться и другие сопутствующие симптомы. Так, при химических ожогах щелочами травмирование кровеносных сосудов сопровождается кровотечением и формированием гематомы. Если же повреждены нервные окончания у пациента может быть нарушена чувствительность тканей или, наоборот, он будет испытывать сильную жгучую боль от легкого соприкосновения с раной.
дальнейшее чтение
Нейтрализация рассматривается в большинстве общих учебников химии. Подробные описания можно найти в учебниках по аналитической химии, таких как
Скуг, Д.А.; Запад, DM; Холлер, JF; Крауч, SR (2004). Основы аналитической химии (8-е изд.). Томсон Брукс / Коул. ISBN 0-03-035523-0. Главы 14, 15 и 16
Приложения
- Штумм, В .; Морган, Дж. Дж. (1996). . Нью-Йорк: Вили. ISBN 0-471-05196-9.
- Snoeyink, VL; Дженкинс, Д. (1980). Водная химия: химические равновесия и скорости в природных водах . Нью-Йорк: Вили. ISBN 0-471-51185-4.
- Миллеро, FJ (2006). Химическая океанография (3-е изд.). Лондон: Тейлор и Фрэнсис. ISBN 0-8493-2280-4.
- Меткалф и Эдди. Очистка, очистка и повторное использование сточных вод . 4-е изд. Нью-Йорк: Макгроу-Хилл, 2003. 526-532.
Чем нейтрализовать щелочь на коже?
Особенность щелочи заключается в том, что щелочь еще некоторое время может воздействовать на кожу, даже если следов самого вещества уже нет. Поэтому, когда пораженный участок кожи промыт водой, его следует обработать раствором уксуса. Данная кислота прекрасно нейтрализует остатки щелочи.
Если ожог небольшой, то после промывания водой и уксусом можно самостоятельно использовать различные лекарства, ускоряющие заживление. Подойдет недорогая мазь Левомеколь, которая оказывает противомикробное действие и устраняет воспаление.
Если появилась гноящаяся рана, то поможет Левосин. Мазь также усиливает регенерационные процессы кожи.
Важно отметить, что использование препаратов актуально лишь в случае отсутствия осложнений. Кожа, которая долго не заживает после щелочного ожога или приобрела неестественный цвет, является сигналом для настороженности и квалифицированного лечения
Выходит, что попадание щелочи на кожу может вызвать долго заживаемый ожог с осложнениями. Просто промыть рану и обработать ее бывает недостаточно. Особенно если концентрация вещества была высокой или повреждена значительная площадь кожи. В этом случае не обойтись без помощи врача.
Видео: срочная помощь при химическом ожоге
В этом ролике врач Ирина Васильченко расскажет, что нужно сделать в первую очередь при попадании на кожу щелочи, чем нейтрализовать ее:
https://youtube.com/watch?v=ukVs_ujP-Tg
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования
Обратите внимание, что цифры в скобках (, и т. д.) являются интерактивными ссылками на такие исследования
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Повреждение тканей, именуемое ожогом, может быть следствием воздействия термических факторов, электрического тока, радиоактивных лучей, а также некоторых химических веществ. Ожог щелочью относится к разряду химических ожогов (Т26-Т28 по МКБ-10).
, , , , , , ,
Об истории открытия
Первые записи о соде фиксируются в воспоминаниях римского врача Диоскорида Педания, который рассказал о способе получения гидрокарбоната натрия методом его упаривания из озёрной воды.
Сода, созданная искусственным путём, впервые появилась лишь в XVIII веке, благодаря научным исследованиям и опытам французского учёного А. Л. Люамеля де Монсо. В 1736 году, методом кристаллизации он получил именно тот порошок, который до сегодняшнего дня широко используется во многих сферах деятельности человека.
В промышленности пищевая сода была получена именно в России. Этому послужило открытие одного из химиков – Эрика Лаксмана, который выяснил, что содовый порошок можно добыть, если спечь природный сульфат натрия и древесный уголь. Методика была опробована на заводе по изготовлению стекла в Тальцинске, однако широкой популярности она так и не обрела.

В 1791 году состоялась вторая, более удачная попытка, в основу которой легло получение соды посредством сплавления древесного угля, смеси сульфата натрия и мела. Данная заслуга принадлежит французскому химику Н. Лебману. После открытия, сделанного им, было создано предприятие, которое ежедневно производило до 120 кг содового порошка. Технология распространилась по всей Европе, и в России в 1864 году также впервые появился завод подобного типа. Предприятие было создано М. Прагом в Барнауле, а спустя некоторое время появился второй, но уже более крупный завод, который ежегодно давал до 20 тысяч тонн пищевой соды. Производство на данном предприятии велось на другой технологии, которая официально была утверждена в 1838-1840-х гг и основывалось на аммиачной методике, позволяющей получать более высококачественный содовый порошок. Постепенно, к 1920 году все предприятия, которые работали по лебмановской методике, были закрыты.